細(xì)胞免疫治療趨勢(shì)
隨著細(xì)胞免疫治療的蓬勃發(fā)展和臨床試驗(yàn)的井噴,各種新興的細(xì)胞藥物給腫瘤治療領(lǐng)域帶來(lái)了質(zhì)的飛躍。截止2022年4月15日,全球腫瘤免疫治療在研管線中有2756種細(xì)胞治療藥物,相比2021年的2031種細(xì)胞療法藥物,有36%的增長(zhǎng)[1]。其中,以嵌合抗原受體T(CAR-T)細(xì)胞療法為代表的技術(shù)迅速改變了血液系統(tǒng)惡性腫瘤的發(fā)展趨勢(shì),并已占目前正在開發(fā)或市場(chǎng)上細(xì)胞療法的一半以上。

圖源:參考文獻(xiàn)1
今年2月,“CAR-T之父”Carl June教授領(lǐng)銜的團(tuán)隊(duì)在《自然》發(fā)表了一篇關(guān)于CAR-T療法的重要論文,通過(guò)長(zhǎng)期研究發(fā)現(xiàn),CAR-T療法的效果可以持續(xù)10年之久[2]!截至目前,美國(guó)FDA批準(zhǔn)了六款產(chǎn)品上市,而國(guó)內(nèi)也在2021年上市了兩款CAR-T細(xì)胞治療藥品。這一療法的商業(yè)化,給“癌癥能否被治愈”這一困擾人類的難題帶來(lái)了一個(gè)新的解決方案。

主流的細(xì)胞療法概覽
臨床試驗(yàn)中最常見的細(xì)胞療法包括:CAR-T細(xì)胞療法、TCR-T細(xì)胞療法、TIL療法、NK細(xì)胞療法以及誘導(dǎo)多能干細(xì)胞源(iPSC)的細(xì)胞療法。其中,CAR-T細(xì)胞療法在血液瘤取得了矚目的成就,正在向攻克實(shí)體瘤努力,TCR-T和TIL在某些實(shí)體瘤中的表現(xiàn)讓人興奮,NK和iPSC也展現(xiàn)巨大的潛力。
1、CAR-T細(xì)胞療法
CAR-T細(xì)胞療法使用患者自身的T細(xì)胞,在體外改造后帶上精準(zhǔn)靶向腫瘤細(xì)胞的嵌合抗原受體(CAR),然后回輸?shù)交颊唧w內(nèi),用于識(shí)別和攻擊腫瘤。由于使用患者自身的T細(xì)胞,可以防止宿主免疫系統(tǒng)的排斥。但同時(shí),體外對(duì)T細(xì)胞進(jìn)行改造和擴(kuò)增需要3-4周的時(shí)間,且屬于定制產(chǎn)品很難標(biāo)準(zhǔn)化。因此,“現(xiàn)貨型”CAR-T細(xì)胞是目前的一大研究趨勢(shì)。
2、TCR-T細(xì)胞療法
TCR-T跟CAR-T細(xì)胞療法一樣都涉及T細(xì)胞表面的抗體改造,二者區(qū)別在于,CAR-T細(xì)胞靶向表面抗原,不受MHC類別限制;而TCR-T細(xì)胞,通過(guò)MHC依賴的方式靶向表面和胞內(nèi)靶點(diǎn)。
3、TIL細(xì)胞療法
腫瘤內(nèi)部或附近的淋巴細(xì)胞已經(jīng)具有識(shí)別和殺傷腫瘤細(xì)胞的能力,通過(guò)體外分離擴(kuò)增并回輸至病人體內(nèi),可以擴(kuò)大免疫應(yīng)答,加強(qiáng)腫瘤殺傷作用,即是TIL療法的原理。與CAR-T療法的區(qū)別如下圖:
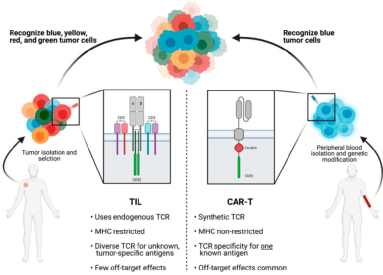
圖源:參考文獻(xiàn)3
4、NK細(xì)胞療法
NK細(xì)胞與T細(xì)胞不同,它們直接檢測(cè)并摧毀受感染和惡性細(xì)胞,而不必被激活或“訓(xùn)練”以對(duì)癌細(xì)胞作出反應(yīng)。根據(jù)思路的不同,可分為經(jīng)過(guò)IL-2、IL-15等細(xì)胞因子的活化處理的NK細(xì)胞和基因工程化NK細(xì)胞(如CAR-NK)。
5、iPSC
iPSC是指利用病毒或非病毒載體技術(shù)對(duì)已分化的成體細(xì)胞進(jìn)行重編程所獲得的具有多向分化潛能的干細(xì)胞,具有類似于人胚干細(xì)胞的多能性。在培養(yǎng)過(guò)程中通過(guò)加入特定誘導(dǎo)因子進(jìn)行刺激及定向誘導(dǎo),可將iPS細(xì)胞誘導(dǎo)分化為目標(biāo)細(xì)胞,如iPSC來(lái)源MSC用于骨關(guān)節(jié)炎的治療、iPSC來(lái)源的NK細(xì)胞療法、iPSC來(lái)源的CAR-T細(xì)胞療法等。
細(xì)胞療法開發(fā)的主要挑戰(zhàn)
盡管近年來(lái)細(xì)胞療法取得了顯著的臨床進(jìn)展和商業(yè)成功,多種療法發(fā)展勢(shì)頭良好。但我們也要看到目前依舊存在許多挑戰(zhàn),例如,細(xì)胞來(lái)源問題、安全性的保障、降低與宿主免疫系統(tǒng)的不良反應(yīng)以及可及性和可支付性的問題。
-->目前上市的細(xì)胞療法都為自體T細(xì)胞療法,從患者體內(nèi)獲得的種子細(xì)胞難以保證質(zhì)量,經(jīng)過(guò)細(xì)胞純化、基因改造、規(guī)模化擴(kuò)增,冷凍保存到臨床使用,是一個(gè)復(fù)雜且必須保證細(xì)胞的關(guān)鍵質(zhì)量屬性的過(guò)程,這也是細(xì)胞臨床治療成功的關(guān)鍵。
-->細(xì)胞療法另一個(gè)挑戰(zhàn)是安全性,包括產(chǎn)品生產(chǎn)過(guò)程異質(zhì)性和關(guān)鍵質(zhì)量屬性的變化、輸注后不良反應(yīng)的控制及長(zhǎng)期在體的安全性。供體不同引起的細(xì)胞異質(zhì)性、工藝不同引起的產(chǎn)品異質(zhì)性和患者疾病微環(huán)境不同引起的治療異質(zhì)性及在細(xì)胞制造工藝中引入異質(zhì)性都有可能引起宿主的細(xì)胞因子風(fēng)暴和神經(jīng)毒性作用。
-->目前上市的產(chǎn)品價(jià)格高昂,在個(gè)人定制療法的前提下很難降低成本,雖然已有不少商業(yè)險(xiǎn)涵蓋了細(xì)胞療法,但其可及性可支付性將是一個(gè)長(zhǎng)期困擾產(chǎn)品普遍應(yīng)用的因素。
細(xì)胞療法的發(fā)展趨勢(shì)
為了應(yīng)對(duì)細(xì)胞治療中的上述挑戰(zhàn),主要有以下幾個(gè)研究方向:
1、通用型細(xì)胞療法的研發(fā)
為了解決自體細(xì)胞療法的諸多問題,“現(xiàn)貨型”通用細(xì)胞療法成為助攻方向,包括通用型T細(xì)胞療法、體內(nèi)T細(xì)胞療法、iPSC來(lái)源的免疫細(xì)胞療法等,在解決生產(chǎn)耗時(shí)過(guò)長(zhǎng)、工藝難以規(guī)范、產(chǎn)能難以提高及生產(chǎn)成本昂貴方面有明顯的優(yōu)勢(shì),有望提高細(xì)胞療法的可及性。
2、安全性的解決策略
通過(guò)沉默在CRS中發(fā)揮重要作用的細(xì)胞因子的shRNA以抑制細(xì)胞因子的釋放,提高安全性;使用非基因編輯工具來(lái)減少脫靶風(fēng)險(xiǎn),使用非病毒載體來(lái)實(shí)現(xiàn)快速編輯持久性應(yīng)答;使用如含海藻酸鹽的凝膠MASTER等半滲透性生物材料和水凝膠來(lái)改善治療細(xì)胞的輸送、活力、保存和安全性;通過(guò)對(duì)CAR結(jié)構(gòu)的改造(如雙特異性CAR)來(lái)減少?gòu)?fù)發(fā)風(fēng)險(xiǎn)和阻止副作用的發(fā)生。
3、攻克實(shí)體瘤
由于缺乏特異性的癌細(xì)胞表面靶點(diǎn),CAR-T細(xì)胞進(jìn)入實(shí)體瘤組織困難,難以浸潤(rùn)腫瘤組織以及腫瘤微環(huán)境對(duì)CAR-T細(xì)胞的免疫抑制等,CAR-T細(xì)胞療法運(yùn)用于實(shí)體瘤治療的進(jìn)展并不順利,而這也是研究人員的突破方向。胃癌中CLDN18.2靶點(diǎn)的運(yùn)用已取得突破,NKG2DL、GUCY2C、MUC1*、MSLN等靶點(diǎn)也取得可喜進(jìn)展。此外,TCR-T細(xì)胞療法在軟組織肉瘤和默克爾細(xì)胞癌也帶來(lái)突破進(jìn)展,TIL療法今年有可能實(shí)現(xiàn)第一款產(chǎn)品的上市等等,某些實(shí)體瘤的攻克已近在眼前。
總結(jié)
細(xì)胞療法是目前腫瘤免疫治療中發(fā)展最快、應(yīng)用最廣的研究熱點(diǎn),已上市細(xì)胞治療產(chǎn)品獲得了不錯(cuò)的成效,而更多產(chǎn)品正在積極的臨床研究中。為了推進(jìn)細(xì)胞治療行業(yè)“產(chǎn)學(xué)研醫(yī)”深度交流,共促行業(yè)穩(wěn)健發(fā)展,生物谷將于9月20-21日舉辦“第十三屆細(xì)胞治療大會(huì)”,邀您共話細(xì)胞治療新未來(lái)。
參考文獻(xiàn):
[1]Saez-Ibañez AR, Upadhaya S, Partridge T, Shah M, Correa D, Campbell J. Landscape of cancer cell therapies: trends and real-world data. Nat Rev Drug Discov. 2022 Jun 1. doi: 10.1038/d41573-022-00095-1. Epub ahead of print. PMID: 35650421.
[2]Melenhorst, J.J., Chen, G.M., Wang, M. et al. Decade-long leukaemia remissions with persistence of CD4+ CAR T cells. Nature (2022). https://doi.org/10.1038/s41586-021-04390-6
[3] Qin S S , Melucci A D , AC Chacon, et al. Adoptive T Cell Therapy for Solid Tumors: Pathway to Personalized Standard of Care[J]. Cells, 10(4):808.
| 版權(quán)聲明: 1.依據(jù)《服務(wù)條款》,本網(wǎng)頁(yè)發(fā)布的原創(chuàng)作品,版權(quán)歸發(fā)布者(即注冊(cè)用戶)所有;本網(wǎng)頁(yè)發(fā)布的轉(zhuǎn)載作品,由發(fā)布者按照互聯(lián)網(wǎng)精神進(jìn)行分享,遵守相關(guān)法律法規(guī),無(wú)商業(yè)獲利行為,無(wú)版權(quán)糾紛。 2.本網(wǎng)頁(yè)是第三方信息存儲(chǔ)空間,阿酷公司是網(wǎng)絡(luò)服務(wù)提供者,服務(wù)對(duì)象為注冊(cè)用戶。該項(xiàng)服務(wù)免費(fèi),阿酷公司不向注冊(cè)用戶收取任何費(fèi)用。 名稱:阿酷(北京)科技發(fā)展有限公司 聯(lián)系人:李女士,QQ468780427 網(wǎng)絡(luò)地址:www.arkoo.com 3.本網(wǎng)頁(yè)參與各方的所有行為,完全遵守《信息網(wǎng)絡(luò)傳播權(quán)保護(hù)條例》。如有侵權(quán)行為,請(qǐng)權(quán)利人通知阿酷公司,阿酷公司將根據(jù)本條例第二十二條規(guī)定刪除侵權(quán)作品。 |
 m.quanpro.cn
m.quanpro.cn